Вакцинация против против вируса папилломы человека: скандалы,
интриги, увольнения!
С чего все началось и почему разгорелся
конфликт в сообществе "Кокрейн"? В статье подробно
разобрана критика систематического обзора вакцинации
против вируса папилломы человека (ВПЧ), которая и вызвала все
споры. Также вы узнаете о проблемах, с которыми
сталкиваются медики при анализе и оценке различных
профилактических средств, а также о том, какой вывод
можно сделать из истории с вакциной против ВПЧ и
конфликтом в "Кокрейн".
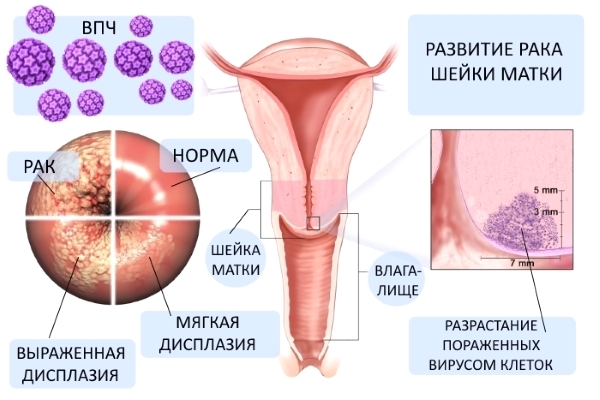
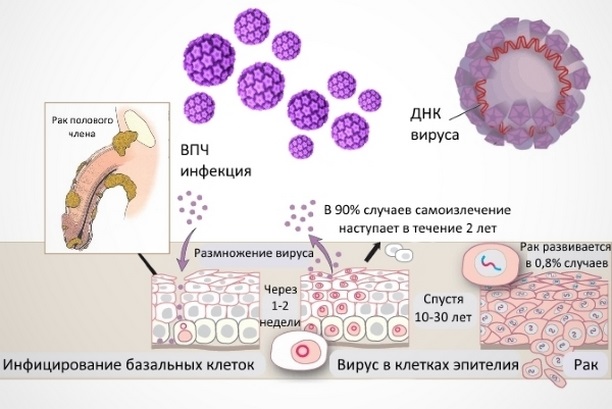
Вирус папилломы человека может вызывать рак половых
органов и глотки
***
Сообщество "Кокрейн" (Cochrane, ранее
Кокрейновское сотрудничество) было основано в 1993 году
в ответ на призыв шотландского врача-эпидемиолога
Арчибальда Кокрейна публиковать систематические обзоры
всех рандомизированных контролируемых исследований в
области здравоохранения. Это одна из самых уважаемых в
мире организаций, занимающихся вопросами доказательной
медицины.
В чем суть конфликта?
В 2018 году внутри сообщества "Кокрейн"
разгорелся скандал: в мае был опубликован обзор Марка
Арбина по вакцинам от вируса папилломы человека (ВПЧ),
которые активно продвигаются фармацевтическими
компаниями как средство профилактики нескольких раков,
прежде всего рака шейки матки. В статье были сделаны
достаточно привычные выводы:
- Вакцинация от ВПЧ пациенток моложе 26 лет уменьшает последующую вероятность предраковых изменений;
- Требуется больше времени, чтобы понять, действительно ли эта вакцинация уменьшает заболеваемость раком;
- Значимых побочных эффектов не найдено;
- В привитой группе общая смертность оказывается выше, но она статистически не значима, а данных для однозначных выводов пока недостаточно.
Всего в обзор попало 26 исследований, в
которых приняли участие 73 428 женщины.
Этот обзор совершенно не устроил Петера
Гётцше (Peter C. Gøtzsche), бывшего на тот момент членом
правления и директором одного из подразделений Кокрейн.
Он и его коллеги в октябре опубликовали критическую
заметку, в которой раскритиковали майский мета-анализ.
Подробнее мы расскажем об этом во второй части статьи,
но основные претензии сводятся к следующему:
В исходный обзор не попала примерно
половина уже законченных исследований этой вакцины;
- Ни в одном из тех 26 исследований, что в
обзор все-таки попали, не было использовано плацебо в
контрольной группе. Вместо плацебо были алюминиевые
адъюванты или другие прививки с адъювантами. При этом в
обзоре говорится о сравнении вакцины с плацебо;
- Значительная часть исследований
учитывала побочные эффекты, проявившиеся только в первые
2 недели после прививки, несмотря на то, что в среднем
наблюдения велись в течение нескольких лет;
- Вероятность общей смертности у пациентов
старше 25 лет, привитых от ВПЧ, статистически значима. В
мета-анализе ее искусственно уменьшили, объединив
различные группы пациентов.
В результате осенью Петера вынудили
покинуть сообщество, что он и сделал, обвинив Кокрейн в
отклонении от первоначальных целей и сотрудничестве с
фармацевтическими компаниями.
***
Читайте также по теме:
***
Чему обрадовались антипрививочники?
Как ни странно, эта история привлекла
внимание антипрививочного движения. В середине февраля в
социальных сетях распространилась информация о том, что
известный ученый Петер Гётцше выступит в США
на конференции, организованной активными противниками
вакцин. В цивилизованном научном мире этому немного
удивились, а кто-то даже пошутил, что Петер отправился
"во все тяжкие" после изгнания из сотрудничества.
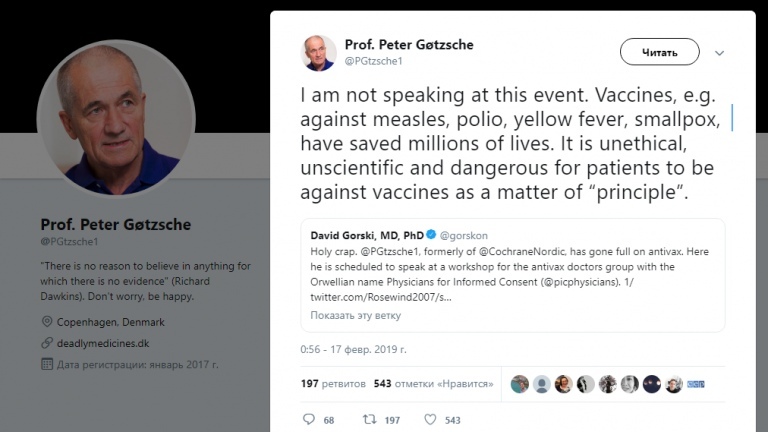
Конечно же, вскоре вышел твит Петера с
отказом от участия в конференции и уточнением, что
вакцины спасли миллионы жизни. Для примера Петер
упомянул корь, полиомиелит, желтую лихорадку и оспу.
К сожалению, это уже не первый случай,
когда результаты и обсуждение мета-анализов, считающихся
вершиной пирамиды доказательной медицины, используются
там, где их точно никто не ожидал увидеть, и приводят к
совсем псевдонаучным выводам и отрицательным
последствиям.
В качестве другого примера можно
вспомнить историю с термографией. В начале XXI столетия
Петер Гётцше активно занимался вопросами скрининга рака
молочной железы и даже опубликовал мета-анализ, в
котором поставил под сомнение методологическую
достоверность большинства исследований и пришел к
выводу, что этот скрининг не снижает смертность.
Значительная часть научного сообщества оставалась не
согласна с этим выводом, в результате сообщество Кокрейн
пошло на компромисс и заменило формулировки в статье.
Акцент был сделан не на отсутствие эффективности, а на
возможный вред от скрининга, так что история постепенно
замялась. Но это не помешало адептам совершенно
бессмысленной "термографии" в диагностике рака
размещать видео с Петером Гётцше, где он рассказывает
про вред маммографии, и сопровождать все это призывами
сделать безопасную термографию.
***
В мае 2018 года сообществом Кокрейн был
опубликован обзор о влиянии вакцин против вируса
папилломы человека (ВПЧ) на развитие рака шейки матки, а
уже в октябре вышла критика этого обзора, ставшая
причиной всех последующих перипетий в сообществе
Кокрейн. Как мы уже знаем, автором критики была группа
исследователей во главе с Петером Гётцше. К сожалению, в
своем разборе оригинального анализа, который, конечно,
не был идеален, они и сами-то были не очень точны и
аккуратны в подсчетах и формулировках. Хорошую "критику
критики", о которой стоит подробно рассказать, сделала
Хильда Бастиан в блоге издательства PLOS. Хильда
рассмотрела основные пункты замечаний Гётцше и коллег,
чтобы понять, кто все-таки прав. Суммируем кратко
основные тезисы.
Авторы оригинального обзора упустили около половины
исследований, поэтому доверять результатам обзора нельзя
Копенгагенская группа (как Хильда
называет Гётцше, Йоргенсена и Джефферсона) обвинила
авторов Кокрейновского обзора в том, что в анализ были
включены только 26 из 46 возможных исследований, которые
удалось найти авторам критики. Довольно серьезное
замечание: не половина конечно, как
они заявили изначально, но все же. Но Гётцше и коллеги
привели список забытых Кокрейновским обзором
исследований не сразу, а уже в ходе ответов на
комментарии к их статье. В итоге, в списке "пропущенных"
оказалось 21 исследование. При этом, 7 исследований лишь
возможно подходили под включение в обзор, еще 3 были на
самом деле включены в анализ эффективности, но не в
анализ нежелательных эффектов. Таким образом, из 21
остается только 11 пропущенных.
Если внимательно посмотреть на
оставшиеся исследования, то интерес с точки зрения
правильности результатов обзора представляет, на самом
деле, только одно, так как в нем принимало участие 20
тысяч человек. Другие 10 исследований в сумме дают
только 5 тысяч человек. Однако большое финское
исследование на 20 тысяч человек авторы Кокрейновского
обзора упоминали, но оно было исключено из анализа, так
как являлось исследованием 4 фазы, а критерии включения
в обзор подразумевали только исследования 2 и 3 фазы.
Датчане обнаружили промежуточный отчет, в котором это
исследование упоминается как 3/4 фазы, хотя во всех
регистрах и публикациях оно относится к 4 фазе, после
чего предложили учитывать эти результаты в анализе.
Дальше вопрос скорее философский - включать исследование
или нет? Протокол обзора и мета-анализа был опубликован
за несколько лет до публикации результатов, уже там
авторы обзора настаивают, что исследования 4 фазы - это
критерий исключения. Говорить о том, что оно было
злонамеренно пропущено, в этом случае будет некорректно.
Почему нельзя включать в обзор постмаркетинговые
исследования? Скорее всего, такая практика существует,
потому что исследования 4 фазы хуже контролируются, их
данные меньше публикуются, а результаты могут содержать
ошибки.
Итого, с учетом вышесказанного, в
исходном мета-анализе было учтено 73 428 участников
исследований из возможных 103 500. А если убрать то
злосчастное исследование 4 фазы, то останется 73 428
участников из примерно 80 000 возможных. И та, и другая
цифры явно не дотягивают до половины, как было заявлено
в одном из пунктов критики. При этом следует отметить,
что авторы обзора уточнили, что не использовали регистры
для поиска исследований, а ориентировались на
полноценные публикации. Тем не менее, они согласились,
что еще 5 исследований можно было бы включить, если бы
они использовали регистры, после чего оперативно сделали
новые расчеты с использованием новых данных, которые
никак не повлияли на результаты.
Авторы обзора игнорируют проблемы
плацебо
Проблема плацебо - это извечная проблема
исследований вакцин, где в качестве контроля приходится
использовать другую вакцину или адъювант от вакцины.
Вопрос тут по сути не к обзору, а к терминологии,
принятой в таких исследованиях. Критики посвятили целый
абзац объяснению неправильной трактовки слова "плацебо".
Надо ли было об этом писать в самом обзоре - да, надо,
но авторы это сделали. Критикам, по-факту, не
понравилось, что об этом было написано мало и не в самом
начале. Возможно, нужно этому уделять больше внимания,
но такой пункт точно не может быть основой для критики
всего исследования.
Авторы обзора изучают суррогатный исход,
то есть снижение количества дисплазий, а не снижение
смертности от рака
По идее, дисплазия - это предраковое
состояние, поэтому снижая риск развития дисплазий, мы
снижаем риск рака. Критики замечают, что большинство
дисплазий не приводят к инвазивному раку. Это
действительно так, но также верно, что практически все
опухоли берут начало от дисплазий, процесс появления
опухоли многоэтапный. Дальше следует оценивать баланс
пользы и вреда от вакцинации, что и пытаются сделать
авторы Кокрейновского обзора. Дисплазия шейки матки
часто не имеет симптомов, но защита от нее позволит
избавиться от череды бесконечных обследований и
вмешательств при скрининге, поэтому если прививка
предотвращает ВПЧ и дисплазию, то это уже положительный
результат.
Критика скрининга также строилась Гётцше
на факте отсутствия данных о снижении риска рака шейки
матки. В данной ситуации используется такая же риторика,
что и при критике скрининга рака за отсутствие данных о
снижении общей смертности, о чем будет подробнее
рассказано в третьей части статьи.
Авторы обзора несерьезно и неправильно
подошли к оценке серьезных побочных эффектов
С побочными эффектами вышла совсем
несостыковка. Авторы критики написали, что пересчитали
нежелательные явления для одного из исследований в
мета-анализе и выяснили, что их было больше, чем учтено
в обзоре. Но если внимательно приглядеться, то авторы
мета-анализа считали участников с серьезными побочными
эффектами (у одного человека может быть несколько
эффектов), а вот авторы критики считали сами явления, а
не людей. Уже это делает критику правильности расчета
побочных явлений от вакцинации немного сомнительной.
Копенгагенская группа, по сути, говорит, что надо было
считать исключительно их способом, но это делает критику
совсем уж похожей на попытку просто придраться.
Авторы не учли важные "сигналы" о
безопасности
"Сигналы" о безопасности - это сообщения
о нежелательных явлениях, которые могут поступать в виде
единичных сообщений или серии наблюдений. Если сигналов
становится много, то это повод разбираться в них. Но
есть и другая сторона "сигналов": часто сообщения
поступают либо не о реальных побочных эффектах, либо о
побочных эффектах, не связанных с вакцинами. Часто
расследования сигналов ни к чему не приводят, но
являются отличной базой для движения против вакцин.
Но самое главное, в задачи мета-анализа
не входит оценка и анализ подобных редких явлений,
которые не являются частью рандомизированных
исследований, а также предположений о возможных побочных
явлениях из всего массива научной литературы. Задача
обзора - обобщить массив данных из исследований, тогда
как единичные побочные явления, если они и есть в
рандомизированных исследованиях, будут выпадать из-за
отсутствия хоть какой статистической значимости. Редкие
нежелательные явления нельзя игнорировать, их надо
изучать, для этого существуют свои методы и
исследования, но это не предмет для конкретного
мета-анализа, поэтому этот пункт критики звучит как
минимум странно. С изучением "сигналов" тоже есть
проблемы, но это совсем другая история. Приведение же в
пример сомнительных кейсов как раз характерно для
антивакцинаторского движения, к которому некоторые блоги
относят и одного из авторов критики, Томаса Джефферсона.
Был конфликт интересов с индустрией
Конфликт интересов - еще одна тема для
обсуждения, привязывать которую к результатам
конкретного обзора довольно странно. Информация о
конфликте интересов авторов была. А подробнее о
конфликте интересов можно прочитать в статье Хильды
Бастиан.
Также в критике были замечания к
пресс-релизу и тому, как подавались результаты обзора в
прессе. Пожалуй, этот пункт заслуживает меньше всего
внимания, так как больше отражает субъективную позицию
критиков, нежели какие-то объективные проблемы. Желающие
могут самостоятельно решить, насколько сообщения в
прессе соответствуют содержанию обзора. Но для этого,
прежде всего, надо прочитать сам обзор.
Важное замечание: авторы критики не
утверждают, что доказательств эффективности вакцин нет
(хотя немного об этом говорят в 3 пункте), а лишь
пытаются оценить методологические проблемы обзора. В
итоге, сама критика вышла так себе и вызвала больше
недоверия к ее авторам, чем к критикуемому обзору. В
отличие от кейса со скринингом рака молочной железы,
аргументы против обзора по вакцинации от ВПЧ были
намного слабее и менее убедительны.
***
Сколько должно быть участников
исследования, и что считать конечными точками?
Когда мы изучаем новое лекарство или
новую методику, призванную снизить смертность, мы
требуем результатов сравнения общей выживаемости. Но
если их нет, то мы часто сомневаемся в правомерности
других суррогатных конечных точек
исследований. ("Суррогатной" конечной точкой в
клиническом исследовании называют лабораторный
показатель или параметр состояния пациента, для которого
доказана или предполагается связь с истинными конечными
точками. Суррогатные точки используются, если достижение
клинических конечных точек требует много времени.
Например, суррогатной конечной точкой испытаний может
стать артериальное давление, так как оно является
фактором риска развития сердечного приступа. Однако само
по себе артериальное давление может не иметь особого
значения для пациентов. - Прим.ред.).
Суррогатная точка, которая была выбрана
при изучении вакцинации - это дисплазия шейки матки
разной степени, по сути, предраковые изменения.
Предраковые изменения не всегда приводят к раку, чем
меньше они выражены, тем выше шанс, что пациент
выздоровеет, а не заболеет раком. С одной стороны,
дисплазия шейки матки довольно далека от такой конечной
точки, как смерть от рака, поэтому и вызвала у критиков
сомнения. С другой стороны, дисплазия - это обязательное
событие на пути от здоровых тканей к инвазивному
неизлечимому раку шейки матки, а при наличии выраженной
дисплазии вероятность развития онкологического
заболевания очень высока.
Давайте представим, что мы решили
доказать, что вакцинация снижает риск умереть от рака
шейки матки, тогда истинной конечной точкой будет
летальный исход. Нам нужно запланировать исследование и
решить, какое количество участников придется в него
включить. Также допустим, что вакцинацию проводят среди
пациенток в возрасте до 15 лет с расчетом на то, что в
будущем снизится смертность.
Первая проблема - это период наблюдения
в исследовании. Минимальный период наблюдения в таком
исследовании должен составлять более 10-20 лет, а еще
лучше 20-30 лет. Почему так долго? Смерти от рака шейки
матки в странах Северной Европы регистрируются у
пациенток старше 25 лет, а чаще - старше 30 лет. В
России такая же картина, только при сравнении со
странами Северной Европы в разных возрастных группах
смертность примерно в 5-8 раз выше. Если в 2015 году в
возрасте 30-39 лет в Норвегии было зарегистрировано 4
смерти от рака шейки матки или 1 смерть на 100 000
человек, то в России было 834 смерти (или 7 случаев на
100 000), то есть в 7 раз больше.
Сначала рассмотрим проведение
исследования в Северной Европе. Добавим в статистику
менее благополучные Данию и Швецию, тогда смертность в
возрасте 30-39 лет составит уже не 1, а 2 случая на 100
000. Возьмем самый оптимистичный прогноз: вакцинация
снижает смертность в 10 раз. Если это так, то среди
вакцинированных смертность от рака шейки матки будет 2
на 1 000 000, а не 2 на 100 000 человек. Поскольку мы
хотим следовать методам доказательной медицины, при
расчете выборки для исследования нас интересует как
минимум двусторонняя ошибка alpha = 0,05 и ошибка
второго рода beta=0,2. С их помощью мы можем рассчитать
достаточную выборку для нашего гипотетического
исследования. Выходит, чтобы доказать, что вакцинация
снижает смертность в 10 раз, количество участников
исследования должно быть больше 1 000 000 - при этом в
каждой из групп, вакцинации и контроля, будет более 500
000 участников. Если же ожидаемое снижение смертности
меньше десятикратного, то выборка должна быть еще
больше.
Теперь предположим, что мы решили
провести такое же исследование в России, тогда все
немного проще. Дело в том, что из-за более высокой
смертности будет достаточно, если в каждой из групп
окажется хотя бы 100 000 человек, значит всего в
исследовании должны принять участие не менее 200 000
пациенток. Но это верно, если мы по-прежнему будем
допускать, что вакцинация снижает смертность в 10 раз и
более, а не менее. И речь все еще идет только об одном
исследовании!
В мета-анализе от сообщества Кокрейн,
который подвергся активной критике со стороны Питера
Гётцше, были данные о всего 73 428 участницах, если
просуммировать все включенные в обзор исследования. Даже
если добавить туда исследования, которые авторы
мета-анализа якобы пропустили (об этом мы писали
подробно во второй части), получится максимум 121 704
человек, плюс-минус 60 000 в каждой группе. Другими
словами, реалистичность проведения исследований по
снижению смертности в результате вакцинации крайне
сомнительна, поэтому без суррогатных конечных точек (в
данном случае - дисплазий различной степени) обойтись
никак не получится.

А нужна ли вообще вакцинация от ВПЧ?
Возникает резонный вопрос, а зачем нам
вообще такая вакцина, если она даже в теории
предотвращает лишь небольшое количество смертей? Но это
вопрос уже не доказательной медицины, а приоритетов в
системе здравоохранения. И тут следует обсуждать
количество смертей в контексте. В России смертность
женщин в возрасте 30-39 лет в 2015 году составляла
примерно 200 на 100 000 человек, однако эта статистика
включает все возможные причины, не только болезни. Из
этих 200 смертей примерно 7 - от рака шейки матки,
довольно редкого в целом онкологического заболевания.
Таким образом, около 3,5% смертей в возрасте 30-39 лет
приходится на одно единственное заболевание, которое
можно предотвратить. Другая проблема, о которой не
говорят в отношении рака шейки матки - это количество
заболевших. А их в возрасте 30-39 лет уже 27 на 100 000
женщин! C учетом того, что только треть из всех случаев
рака шейки матки выявляется на ранних стадиях,
оставшихся пациенток ждет впоследствии большая операция
или комбинированное лечение.
В странах Северной Европы и в Австралии
вакцинация против ВПЧ является приоритетом не только
из-за рака шейки матки, а из-за всего спектра
онкологических и неонкологических заболеваний, которые
может вызвать этот вирус. Подходить к исследованиям
вакцинации ВПЧ с точки зрения формальных критериев,
применяемых в онкологических исследованиях - заведомо
выигрышный для критиков вариант. Но формальный подход к
методам в той же степени вредит доказательной медицине,
как и полное их игнорирование.
Не так давно были
опубликованы результаты ретроспективного популяционного
исследования в Шотландии. Авторы показали снижение новых
случаев дисплазии шейки матки 3 степени (CIN3+) после
вакцинации на 90% при сравнении двух соседних поколений,
1988 (не вакцинированного) и 1995 (вакцинированного)
годов рождения.
Что в итоге?
Из этой длинной истории следует сделать
несколько выводов.
Во-первых, результатам исходного
мета-анализа, сделанного сообществом Кокрейн, стоит
доверять. Даже с учетом выявленных неточностей и
возможных недочетов, его результаты соответствуют
истине. Это значит, что вакцинация в раннем возрасте
способна предотвратить подавляющее число случаев
предопухолевых изменений шейки матки, рака шейки матки
и, соответственно, смертей от рака шейки матки. Конечно,
вакцина не дает 100% защиту по разным причинам, поэтому
она не отменяет необходимости скрининга рака шейки
матки, но, возможно, упрощает его.
Во-вторых, вероятно вакцина
малоэффективна для женщин после начала половой жизни и
для женщин старшего возраста. Но если какой-то эффект от
вакцинации этих групп и есть, то он точно не достигнет
того же уровня, что и при вакцинация подростков.
Скорее всего вакцина безопасна и у нее
нет значимых серьезных побочных эффектов, кроме
локальной реакции на введение. Но в исследованиях
вакцинации еще много непонятного: сколько доз необходимо
для иммунизации, как долго длится защита, какую долю
населения следует вакцинировать, чтобы возник
популяционный эффект вакцинации, какой эффект от
вакцинации у мальчиков? Все это будет являться предметом
дальнейших исследований.
Во-третьих, к интерпретации результатов
исследований профилактики и скрининга следует относиться
с учетом специфики этих воздействий и редкости изучаемых
исходов. Показано, что рандомизированные исследования
скрининга, в отличие от исследований методов лечения,
могут выявить эффект ниже, чем он есть в реальности.
А еще важно понимать, что большинство
научных работ содержат ошибки и неточности. Процесс их
выявления важен и необходим, но критическая оценка не
должна являться самоцелью. Критика - лишь часть процесса
интерпретации получаемых нами научных знаний в ходе
разработки новых методов профилактики и лечения
заболеваний.
Антон Барчук, онкоэпидемиолог,
научный
сотрудник Университета Тампере и
ФГБУ "НМИЦ онкологии
им. Н.Н. Петрова"
Медфронт - 28.03.2019.
|

